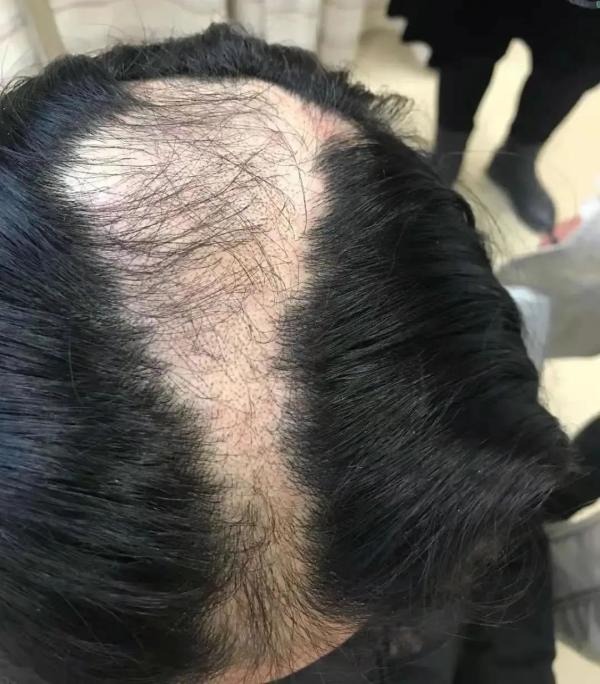
糖尿病引起皮肤瘙痒症的原因有哪些?以及具体表现在哪些方面?
慢性瘙痒(Chronic Pruritus, CP)是一系列皮肤及其他系统性疾病的常见症状。其中,糖尿病性皮肤瘙痒症就是糖尿病常见的皮肤并发症,治疗上除控制血糖水平以外,主要遵循慢性瘙痒的阶梯疗法,但总体疗效欠佳。顽固的瘙痒常常给糖尿病患者造成严重的身心负担。
为更加具有针对性地对其进行防治,已经有许多学者对糖尿病性皮肤瘙痒的发病机制及危险因素做出了研究和总结。

瘙痒是皮肤或黏膜的一种引起搔抓欲望的不愉快的感觉。糖尿病合并皮肤瘙痒症是指糖尿病患者无皮肤原发性损害,而以皮肤瘙痒为主要临床表现的皮肤病,严重者可出现抓痕、血痂、皮肤肥厚和苔藓样变。
长期顽固的瘙痒除了会使患者皮损加重以外,还可能使得患者长期伴随焦虑、抑郁情绪以及睡眠障碍, 增加患者自伤和自杀的风险,有研究提出,糖尿病合并皮肤瘙痒所引起的自伤行为可能是导致糖尿病神经病变截肢的潜在危险因素。
部分患者还可能继发心因性瘙痒、形成瘙痒-搔抓恶性循环等,使得病情进一步加重。
糖尿病性皮肤瘙痒症的发病机制
目前,糖尿病性皮肤瘙痒症的发病机制尚不完全清楚,多数研究认为与长期血糖控制不佳所继发的周围神经及血管损伤、皮肤生理功能异常等因素有关。 糖尿病并发皮肤瘙痒有两个主要原因:皮肤干燥症和糖尿病多发神经病,推测糖尿病性皮肤瘙痒是由于皮肤及神经发生病变后所致。
目前的普遍共识是,痒觉是一种从皮肤开始,由特异性神经介质刺激神经元发放并传递神经冲动后所,在大脑皮层产生的特殊感觉。故而,皮肤上的激发及各级神经元的传导是瘙痒产生的两个重要环节。皮肤是人体最大的器官,含有丰富的血管、神经和独立完整的皮肤免疫系统。
糖尿病患者因长期血浆葡萄糖水平异常升高,体内继发一系列代谢紊乱,糖尿病状态下皮肤生化、皮肤代谢和皮肤免疫系统出现异常,皮肤组织包括角质形成细胞、细胞间质、真皮胶原纤维、神经、血管等均可能受到损伤,皮肤功能减退。
皮肤屏障功能的异常可能影响瘙痒的触发,糖尿病患者周围神经损伤可能干扰正常的痒觉正常传导通路,使得患者更易出现瘙痒。
另外也有研究提出,糖尿病患者体内存在免疫炎症系统紊乱,由于许多炎症介质也参与了痒觉的传导,免疫炎症系统紊乱、 炎症介质水平异常,可能也与糖尿病患者出现皮肤瘙痒有关。
皮肤屏障受损
表皮渗透屏障受损
皮肤渗透屏障由角质形成细胞、细胞间质及缝隙连接组成,各组分都在皮肤水合中起着重要的作用。皮肤物理性屏障功能即表皮渗透屏障功能的减弱是多种瘙痒性皮肤疾病发病的重要环节。
皮肤干燥常被认为是表皮渗透屏障功能受损的表现,主要反映指标为角质层含水量下降,是发生瘙痒的重要原因之一。
糖尿病患者常伴有皮肤干燥,原因可能是多方面的,嘱糖尿病合并皮肤瘙痒患者坚持一段时间外用皮肤保湿剂后,角质层含水量增加的同时,瘙痒也有所减轻。
较健康人群而言,糖尿病患者可能存在一定程度上皮肤屏障功能的异常。研究发现,T2DM患者TEWL值较常人有所升高,角质层水合程度无显著差异。
但糖尿病患者与健康人群的皮肤水合和TEWL值并无显著差异,并且,糖尿病患者的这两项指标会受到患者当下的血糖水平影响,当患者空腹血糖水平升高到某一程度时,其皮肤角质层含水量及TEWL值均会有所降低,且可逆,并指出这一改变与皮肤瘙痒的发病存在一定的相关性。
在此前,糖尿病患者表皮的水分流失也一直被认为是由高血糖和血液高渗引起的,而不是皮肤的水分蒸发。
提示糖尿病患者的确存在表皮水分的流失,但可能并不以向表皮外流失为主,角质层所含水分可能因为高血糖所造成的渗透压差驱动,从而向皮肤生层流动,导致角质层水分含量下降,并出现皮肤干燥。
除高血糖高渗和水分蒸发两条途径导致皮肤水分流式以外,表皮渗透屏障各组成成分的异常也可能引起皮肤水合作用的下降,使得角质层含水量减少,从而导致皮肤干燥、瘙痒。
具体可以从以下几个方面进行总结:①表皮细胞增殖障碍: 糖尿病患者常皮肤菲薄,有研究观察到糖尿病小鼠的表皮厚度的确明显变薄,同时表皮细胞存在一定程度的增殖障碍。
②板层小体减少和脂质含量降低:角质层细胞间脂质具有重要的保湿作用,尤以神经酰胺为主,神经酰胺是重要的天然保湿因子。板层小体是产生细胞间脂质的重要场所。
研究显示,与健康人群相比,2型糖尿病患者表皮中的神经酰胺、脂肪酸和胆固醇含量显著降低,这可能与AGEs的蓄积有关。
③皮脂腺、汗腺萎缩:糖尿病继发周围神经病变会导致皮脂腺和汗腺萎缩,影响出汗,减少皮肤水合。
④其它:角质层中参与形成角化细胞套膜的兜甲蛋白、丝聚蛋白及内披蛋白等成分也可能在AGEs作用的下发生糖基化,结构和功能受到影响,其中,丝聚蛋白是天然保湿因子的重要来源,有助于维持正常的角质层水合功能。
我们在日常建议糖尿病性皮肤瘙痒症患者应注重保湿治疗的同时,也应优先选用含有保湿成分如神经酰胺类物质的润肤油。至关重要的是,也应嘱患者严格监测和控制血糖水平处于正常范围内。
表皮抗菌屏障受损
为了抵御体外病原微生物的入侵,除了需要维持良好的表皮渗透屏障这一基础屏障,还需要表皮维持特定的微生态环境、适宜的酸碱状态以及始终保持有适量抗菌物质,这一系列屏障组成了表皮的一大功能性屏障——抗菌屏障。
研究发现,糖尿病患者发生皮肤感染的概率较健康人群明显升高,且以真菌感染更为常见。另外,糖尿病患者的瘙痒通常发生在局部,尤其是在肛周/生殖器区域,而且多由真菌感染引起。
提示糖尿病患者的表皮抗菌屏障可能存在损伤,从而导致抵御病原微生物入侵和生长的能力下降。
研究发现,糖尿病患者多存在表皮渗透屏障损伤,因此可能会在一定程度上影响表皮抗菌屏障的功能,使得皮肤抵抗病原微生物侵袭的能力下降。
此外,在表皮中,存在一种大量表达的小肽——抗微生物肽(AMPs), 抗微生物肽由表皮深层产生并运送至角质层,在抵抗外来病原微生物的侵袭和维持表皮微生态中起着至关重要的作用。不能忽视的是,表皮抵抗病原微生物入侵还得益于偏酸性的表皮环境。
皮肤pH升高也是老年人发生皮肤瘙痒的主要原因之一,提示表皮的弱酸性屏障受损可能与瘙痒的产生有关, 但具体原因不甚清楚。
糖尿病患者皮肤渗透屏障受损、表皮抗微生物肽含量降低及表皮弱酸性环境被打破,可能使得表皮的抗菌能力显著减弱,从而继发皮肤感染,尤其是真菌感染,可能因此引起严重的皮肤瘙痒。
因此,在糖尿病性皮肤瘙痒症的治疗过程中,注重修复表皮通透屏障的同时,也应重视维护表皮的酸性环境并预防皮肤感染的发生。
糖尿病多发神经病(Diabetic Polyneuropathy,DPN)
特异性神经传导是目前公认的痒觉产生机制,从外周神经系统到中枢神经系统均存在特异性参与痒觉信息处理的神经元。目前,对糖尿病神经病变引发瘙痒的具体机制仍然知之甚少,相应的治疗策略尚不完善。
大量研究证明,瘙痒与糖尿病患者继发周围神经病变存在密切的联系,推测可能是因为神经损伤以后,影响了痒觉正常的神经传导过程。营养神经和抗神经炎治疗可能是缓解和预防糖尿病性皮肤瘙痒的途径之一。
免疫及炎症因素
瘙痒通常由皮肤中的致痒源引起,包括组胺、5-羟色胺、神经肽、细胞因子、炎症产物及某些药物等。其中,促炎因子和炎症介质可直接激活或致敏瘙痒神经元,引起瘙痒,因此,瘙痒受免疫炎症反应的直接影响。
证据表明,在病理状态下,瘙痒相关炎症因子如IL-31、IL-4和NGF反复刺激神经元上与瘙痒信号相关的离子通道TRPV1和TRPA1,导致瘙痒感觉阈值降低,从而引起慢性瘙痒。
目前针对糖尿病性皮肤瘙痒症的多种治疗方法疗效均有限,我们猜测,由于每个患者所处的疾病阶段及自身的个体状况不同,引起瘙痒的主要原因也不同,考虑对本病的治疗应该做出个体化的策略。
然而,首要前提仍然是严格维持正常的血糖水平,从而对各种继发性损害进行有效的预防。目前,其余的治疗,主要还是遵循慢性瘙痒的阶梯疗法,并同时强调皮肤的正确护理。
有研究提出,治疗糖尿病的一些以促炎介质、炎症因子及免疫细胞为靶点的抗炎药物如Tocilizumab可能有助于缓解糖尿病引起的瘙痒,但疗效还有待进一步证实。另外,P2Y12可能是治疗T2DM瘙痒的一个有希望的靶点。
针对糖尿病性皮肤瘙痒症的药物仍然不足,尚需要进一步的研究来提供更多关于有效治疗靶点及用于评价治疗效果的信息。